В России одобрен инновационный препарат для лечения бляшечного псориаза средней и тяжелой степени
- Новости /
-
3379
Препарат Тремфея (гуселькумаб) – это первый одобренный биологический препарат, избирательно блокирующий интерлейкин (ИЛ) -23
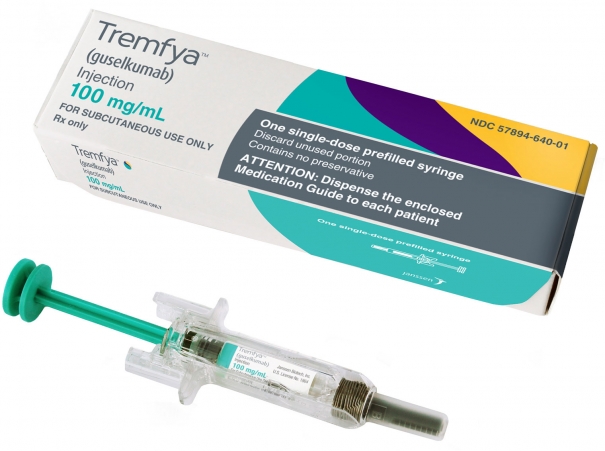
«Янссен», подразделение фармацевтических товаров ООО «Джонсон & Джонсон», объявляет о регистрации в России препарата Тремфея (гуселькумаб), который показан для лечения бляшечного псориаза средней и тяжелой степени у взрослых пациентов, которым показана системная терапия[1].
Гуселькумаб – первый биологический препарат, который избирательно блокирует интерлейкин (ИЛ) -23, ключевой цитокин в воспалительной реакции иммунной системы при псориазе[2],[3],[4],[5]. Терапия с использованием гуселькумаба предполагает две инициирующие инъекции на неделе 0 и 4, затем поддерживающие инъекции 1 раз в 2 месяца1.
Катерина Погодина, управляющий директор «Янссен» Россия и СНГ, генеральный директор ООО «Джонсон & Джонсон», прокомментировала: «Мы гордимся тем, что наш инновационный препарат для лечения псориаза получил одобрение регуляторных органов России и в скором времени будет доступен пациентам в нашей стране. Псориаз – тяжелое системное заболевание, которое откладывает серьёзный негативный отпечаток в первую очередь на качество жизни пациентов[6]. Ключевой показатель успешности терапии псориаза – достижение полного очищения кожи, а также снижение негативного влияния коморбидных состояний на здоровье пациента[7]. Гуселькумаб призван помочь пациентам с тяжелыми формами заболевания, помогая им сохранять достойное качество жизни, социальную активность и трудоспособность3,4,5».
Решение о государственной регистрации было принято Министерством здравоохранения РФ на основе ряда клинических исследований, подтвердивших эффективность и безопасность препарата Тремфея1. В частности, был достигнут высокий уровень очищения кожи, значительное снижение площади распространенности и тяжести течения псориаза, в том числе «проблемной» локализации у пациентов, находящихся на терапии гуселькумабом3, 4.
Алексей Алексеевич Кубанов, Председатель Российского общества дерматовенерологов и косметологов, член-корреспондент РАН, профессор, отметил: «Несколько лет назад Всемирная организация здравоохранения признала псориаз социально значимым заболеванием. Псориаз приносит много страданий пациентам, в том числе и психологических. Регистрация в России новых препаратов для системного лечения значительно расширяет возможности терапии для пациентов, страдающих тяжелыми, часто рецидивирующими формами псориаза. В отношении гуселькумаба можно сказать, что мы ожидаем, что данные об эффективности и безопасности препарата, полученные в ходе клинических исследований, будут продемонстрированы и при широком использовании препарата в ежедневной клинической практике в медицинских организациях дерматологического профиля3,4,5».
В 2017 году препарат Тремфея был одобрен Европейским медицинским агентством на основании данных, полученных в ходе трех клинических исследований фазы III8. Исследования VOYAGE 1 и 2, в ходе которых гуселькумаб сравнивался с плацебо и препаратом адалимумаб, показали высокий уровень очищения кожи уже через 16 недель терапии с 90-процентным снижением Индекса распространённости и тяжести псориаза (PASI 90) у 73,3% и 70,0% пациентов, получавших гуселькумаб (p<0,001 в сравнении с плацебо)3,4. К 24 неделе терапии достижение PASI 90 отмечалось у 80,2% и 75,2% пациентов получавших гуселькумаб по сравнению с 49,7% и 46,8% пациентов, получавших адалимумаб соответственно (P <0,001)3, 4. Высокий результат терапии гуселькумабом сохраняется: спустя 3 года 97,4% пациентов имеет ответ по индеку PASI 75 (значительное очищение кожи)[8].
В исследование NAVIGATE были включены пациенты, у которых не произошло полного или почти полного очищения кожи (по шкале IGA (Общая оценка состояния пациента исследователем) 0 или 1) к 16-й неделе терапии препаратом Стелара ® (устекинумаб), и которые затем были рандомизированы и переключены либо на терапию гуселькумабом, либо остались на терапии устекинумабом4. Среди пациентов, рандомизированных в группу терапии гуселькумаба, доля больных, достигших полного либо почти полного очищения кожи, у которых значение показателя IGA составило 0 или 1, показала значительно более высокое среднее число пациентов, а также показала по крайней мере 2-балльное улучшение индекса в период с 28-й по 40-ю неделю (по отношению к 16-й неделе) была значимо выше по сравнению с группой устекинумаба (1,5 против 0,7, P <0,001)5.
Программа клинических исследований гуселькумаба для лечения псориаза не выявила отчетливых данных о повышении рисков развития злокачественных новообразований, кардиоваскулярных или рисков развития серьезных инфекций, включая туберкулез и реактивацию латентного туберкулеза на фоне приема препарата3,4,5.
Пресс-релиз
[1] Государственный реестр лекарственных средств [Электронный ресурс], URL: http://grls.rosminzdrav.ru/Grls_View_v2.aspx?routingGuid=06e7fa3a-e993-4bad-aa90-f28b2de029d3&t= Дата обращения: 08.08.2019
[2] Blauvelt A and Papp K.A et al. J Am Acad Dermatol 2017;76(3):405–17.
[3] Reich K and Armstrong A.W et al. J Am Acad Dermatol 2017;76(3):418–31
[4] Langley RG et al. Br J Dermatol 2018; 178: 114−123
[5] Bachelez H. The Lancet 2017;390:208–10.
[6] Kerdel F. The Importance of Early Treatment in Psoriasis and Management of Disease Progression. J Drugs Dermatol. 2018 Jul 1;17(7):737-742.
[7] Strober BE et al Clinical Goals and Barriers to Effective Psoriasis Care Dermatol Ther (Heidelb). 2019 Mar;9(1):5-18
8 The European Medicines Agency (EMA) [Электронный ресурс] URL: https://www.ema.europa.eu/en/documents/smop-initial/chmp-summary-positive-opinion-tremfya_en.pdf Дата обращения 05.08.2019
[8] C.E.M Griffiths at al. Presented at Fall Clinical Dermatology congress, 18-21 October 2018, Las Vegas Nevada
.png)