Типы и методы проведения фармакоэкономических исследований

- Библиотека /
-
4713
анализ минимальных затрат или анализ всех издержек,
анализ эффективности и затрат,
анализ полезности и затрат,
анализ затрат и результатов.
Приемлемое соотношение стоимости и эффективности и/или стоимости и полезности в некоторых странах стало необходимым условием включения лекарственных средств в лекарственные формуляры, дотируемые государством.
Ряд исследований по анализу осуществляется путем проведения проспективных клинических испытаний у лиц контрольных групп. Испытуемых включают в группы лечения по принципу случайной выборки, а ход их лечения отслеживают во времени. Эти исследования можно проводить двойным слепым методом. Конечную цель и методы анализа определяют на этапе планирования исследования.
Эффективность использования медицинских услуг в естественных условиях подвергают мониторингу в течение заранее фиксированного времени. Естественные условия являются важной отличительной особенностью научного анализа исходов лечения. При проведении традиционных клинических исследований частоту визитов испытуемых, количество применяемых процедур и вариантов лечения определяют с помощью Протокола исследования. В противоположность этому анализ исходов лечения в естественных условиях предполагает подсчет параметров применения медицинских услуг без учета влияния методов исследования, так как пациенты посещают медицинские учреждения согласно наработанной практике последних. Сбор данных о проспективных клинических исследованиях, проводимых в естественных условиях, может поставить перед исследователями совершенно новые задачи.
Гораздо чаще проводят ретроспективные клинические исследования, подразумевающие анализ данных уже завершенных исследований. Типичным случаем являются отбор и оценка информации о пациентах, получавших интересующее исследователя лечение. На основании данных о результатах двух разных видов лечения составляют 2 группы пациентов. В зависимости от цели исследования анализируют данные, полученные во время визитов к врачу, а также сведения об оказании медицинских услуг иного характера. Такие клинические исследования осуществляются в условиях организованной системы медицинской помощи и при наличии данных о продолжительных клинических исследованиях.
Продолжительные клинические исследования (longitudinal studies) могут быть рандомизированными или нерандомизированными и предполагают наблюдение пациентов в течение продолжительного времени. На рисунке изображены типы фармакоэкономического анализа (см. также табл. 1).
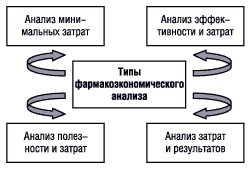 |
Рисунок. Общепринятые типы фармакоэкономического анализа
Таблица 1Типы клинических исследований исходов лечения
Вид анализа | Характеристика исходов лечения | Критерий затрат |
Минимальные затраты (все издержки, стоимость лечения) | Предполагается, что все курсы лечения имеют эквивалентные результаты; исходы лечения не измеряются | Прямые и косвенные эффекты в денежном выражении |
Эффективность и затраты | Описание эффектов, достигаемых посредством обычной клинической практики; группы отражают конкретные случаи | |
Полезность и затраты | Стандартизированные характеристики полезности, в частности, соотношение количества лет продленной жизни и ее качества (QALY) | |
Затраты и результаты | Исходы лечения в денежном выражении |
АНАЛИЗ МИНИМАЛЬНЫХ ЗАТРАТ (CMA — COST-MINIMIZATION ANALYSIS)
По критерию минимальных затрат клинические исследования предназначены для определения меньших затрат на реализацию одного из двух или более методов лечения. Их клиническая эффективность либо известна, либо считается эквивалентной. При проведении таких исследований учитывают все виды медицинского обслуживания, которые относят к каждому методу лечения, и определяют затраты на них.
Минимальные затраты рассчитывают по формулам:
СМА =DC1 – DC2
или
СМА = (DC1+ IC1) – (DC2 + IC2),
где СМА — показатель разницы затрат,
DC1 — прямые затраты при применении 1-го метода,
IC1 — косвенные затраты при применении 1-го метода,
DC2 и IC2 — прямые и косвенные затраты при применении 2-го метода.
Пример клинического исследования с помощью анализа минимальных затрат. Критерий минимальных затрат можно использовать, например, для сравнения двух эффективных гиполипидемических лекарственных средств. При этом накапливают данные о результатах лечения двух групп испытуемых, получающих один из препаратов. Если один из препаратов оказывает большее количество неблагоприятных действий, пациентам могут потребоваться дополнительные визиты в медицинские учреждения. Связанные с этим затраты, включая дополнительные диагностические исследования, обязательно отразятся на повышении стоимости лечения данным препаратом. При проведении клинического исследования розничную цену каждого препарата учитывают с помощью критерия минимальных затрат.
Клиническое исследование, предназначенное для оценки затрат на один метод лечения без сравнения его с каким-либо другим, можно назвать Анализом всех издержек. Исследование, учитывающее все прямые и косвенные затраты на лечение пациента с каким-либо конкретным заболеванием без учета метода лечения, называется Анализом затрат на препарат против конкретной болезни. Полученная в ходе такого анализа информация может оказаться полезной для фармацевтической компании, которая приступает к разработке лекарственного средства, имеющего соответствующие показания. Результаты анализа всех издержек помогают определить, достаточна ли финансовая прибыль, полученная от продажи исследуемого препарата. Эти данные могут также иметь значение при продвижении на рынок лекарственного средства, при использовании которого снижаются затраты на медицинское обслуживание.
АНАЛИЗ ЭФФЕКТИВНОСТИ И ЗАТРАТ (СЕА — COST-EFFECTIVENESS ANALYSIS)
Наиболее привычным и, возможно, наиболее полезным видом клинических исследований исходов лечения является Анализ эффективности и затрат. Сравнивают общие затраты на весь объем медицинских услуг, связанных с разными видами лечения, их клиническими эффектами. Анализ эффективности и затрат основывается на исследованиях, проводимых путем анализа минимальных затрат с учетом как эффективности, так и затратности метода лечения. Это позволяет выделить те виды лечения, которые, вероятно, будут дороже, но которые сбалансированы благодаря более высокой клинической эффективности.
Анализ эффективности и затрат рассчитывают по формуле:СЕА= (DC+IC )/Ef,
где СЕА — соотношение «затраты/эффективность» (выявляет затраты, необходимые на единицу эффективности, например, на одного вылеченного больного),
DC — прямые затраты,
IC — непрямые затраты,
Ef — эффективность лечения (относительное количество вылеченных больных).
Пример исследования с помощью анализа эффективности и затрат. Для сравнения могут быть отобраны два лекарственных средства, предназначенных для лечения пациентов с недержанием мочи. Главной конечной целью определения эффективности лекарственного средства является поддержание определенного уровня качества жизни. Для оценки уровня жизни по стандартной схеме прежде всего отбирают обоснованные показатели, включая субъективную оценку пациента. Еще одной конечной целью является определение затрат на весь объем медицинского обслуживания пациента с недержанием мочи. Сюда обязательно включены визиты к врачу, лабораторные тесты, хирургическое вмешательство, другие дополнительные методы и средства лечения.
Если затраты на лечение оказались сходными, но одна группа пациентов обращалась за помощью к хирургу чаще, чем другая, то результаты лечения по критерию эффективности будут, безусловно, разными. Один из альтернативных вариантов может оказаться более дорогостоящим и тем не менее более эффективным по отношению к затратам. Эффективность затрат не обязательно совпадает с экономией затрат.
Единицы, используемые для измерения эффективности, обычно соотносятся с соответствующими показаниями к использованию лекарственного средства. Для оценки потенциальных результатов лечения обычно применяют систему характеристик, включающую снижение уровня смертельных исходов, выписку из больницы в жизне- и работоспособном состоянии и годы жизни после лечения. Для хронических заболеваний нефатального характера эта система является менее объективной. В этом случае можно использовать характеристики качества жизни больного. Это уместно по отношению к любому заболеванию, снижающему функциональные возможности пациента, в частности, к психическим, неврологическим заболеваниям, болезням органов дыхания. В настоящее время ведется работа по совершенствованию стандартных характеристик, касающихся уровня качества жизни.
Клинические исследования по оценке эффективности затрат имеют серьезные теоретические перспективы, однако на практике их использование ограничено. Проспективные разработки могут оказаться дорогостоящими и требуют много времени. Например, при хронических заболеваниях исследования необходимо продолжать до окончания лечения, хотя для этого может потребоваться много времени. Кроме того, достаточно трудно сформировать группы больных с точными критериями сравнения. Затраты на наблюдение выбранной для сравнения группы больных могут быть сокращены, если есть надежные данные о затратах на лечение, например, информация о результатах предыдущих клинических исследований по критерию минимальных затрат. Однако данные по выбранной для сравнения ретроспективной группе могут уменьшить обоснованность выводов о проведенном клиническом исследовании.
Анализ эффективности и затрат — весьма действенный метод экономической оценки лекарственных средств. Но при этом он имеет два основных недостатка, ограничивающих его применение в определенных условиях: 1) будучи одномерным, метод не может быть использован для сравнения различных видов врачебного вмешательства, которые оказали разное воздействие на состояние здоровья; 2) указывая наиболее эффективный путь действия, метод не позволяет определить свою общественную полезность.
АНАЛИЗ ПОЛЕЗНОСТИ И ЗАТРАТ (CUA — COST-UTILITY ANALYSIS)
Если врачебное вмешательство дает многомерные результаты, экономисты разработали метод анализа по критерию «стоимость—полезность», пытаясь интегрировать данные измерений различных эффектов в одну шкалу.
Анализ полезности и затрат представляет собой тип клинического исследования по критерию эффективности затрат, который переводит клинический исход лечения в плоскость его полезности. Она определяется как некая преференция (предпочтение, преимущество) пациента. Для измерения полезности затрат широко применяют критерий соотношения количества лет продленной жизни к ее качеству (Quality-Adjusted-Life-Years — QALY). Это позволяет охарактеризовать проводимое лечение путем прогнозирования особенностей и качества предстоящей жизни, которые можно ожидать в течение прогнозируемого срока выживания. Другими словами, это сопоставление количества лет жизни с уровнем ее качества на данный срок.
При проведении исследований затраты на лечение сопоставляют с критерием полезности (QALY). Например, исследователи могут определить, что стоимость новой технологии будет составлять 100 тыс. долларов США по отношению к критерию QALY, полученному в результате анализа. При наличии таких данных появляется возможность сравнить разные курсы лечения, опираясь на учет затрат на лечение (сбережение средств) по отношению к критерию QALY.
Полезность и затраты рассчитывают по формулам:
CUA =((DC1 + IC1) – (DC2 + IC2))/(Ut1 – Ut2)
или
CUA = (DC + IС)/Ut,
где CUA — показатель прироста затрат на единицу полезности, соотношение «затраты/полезность» (т.е. стоимость единицы полезности, например, одного года качественной жизни),
DC1 и IC1 — прямые и косвенные затраты при 1-м методе лечения,
DC2 и IC2 — прямые и косвенные затраты при 2-м методе лечения,
Ut1 и Ut2 — утилитарность при 1-м и 2-м методах лечения.
Пример исследования с помощью анализа полезности и затрат. При лечении больных раком мочевого пузыря in situ два лекарственных средства уже доказали свою способность увеличивать период выживаемости: препарат А — на 2 года, препарат В — на 4 года. Однако болевой синдром, обусловленный применением препарата В, снижает способность пациента работать или активно проводить свободное время, в результате чего снижается качество жизни пациента. Ознакомившись с этими данными, некоторые пациенты могут выбрать препарат А, предпочитая жить меньше, но при этом иметь более высокое качество жизни.
Таким образом, акцент делают не только на клинической эффективности, но и на оценке полезности лекарственного средства.
АНАЛИЗ ЗАТРАТ И РЕЗУЛЬТАТОВ (CBA — COST-BENEFIT ANALYSIS)
Следующим видом клинического исследования по критерию эффективности затрат является анализ затрат и результатов. Он позволяет компенсировать второй недостаток анализа эффективности и затрат (СЕА), обусловленный невозможностью оценить общественную ценность лекарственного средства. В этом случае за единицу оценки клинических результатов, полученных с помощью любого метода лечения, принимают денежный эквивалент. Таким образом, прямые затраты на лечение можно сравнивать с денежным выражением непосредственного эффекта, полученного в результате клинического испытания. Такой способ сравнения представляется логичным, однако существуют трудности в оценке подобных результатов: как, например, представить сохраненную жизнь или дополнительные годы жизни в денежном выражении? В силу этих и многих других трудностей анализ затрат и результатов используют редко.
Пример использования анализа затрат и результатов. Были подсчитаны затраты на лечение пациентов с артериальной гипертензией с применением нового метода. Выявлено уменьшение количества смертельных исходов в группе больных, получавших данное лечение, по сравнению с пациентами, не получавшими его. Для проведения анализа по критерию затрат и результатов продление жизни пациента при использовании нового курса лечения необходимо было выразить в долларах, после чего полученный эффект сопоставить с затратами на лечение артериальной гипертензии с применением нового метода.
Перспектива научного исследования определяет план исследования. Научное исследование с использованием фармакоэкономического анализа нужно организовывать и планировать исходя из представления о предстоящей работе. Исследования обычно осуществляют с учетом маркетинговых задач, однако решения, касающиеся оплаты лечения, участники лечебного процесса — пациенты, отдельные врачи, государственные учреждения здравоохранения, третья сторона в лице страховых компаний, а также учреждений, оказывающих медицинскую помощь, принимают по-разному. План клинического исследования и затраты, закладываемые в смету проведения анализа его результатов, должны соответствовать целям и задачам той группы, которая, как ожидается, будет использовать результаты исследования.
Виды затрат. В ходе клинического исследования исходов лечения подсчитывают два вида затрат: прямые и косвенные. Примеры прямых и косвенных затрат приведены в табл. 2. Прямые затраты отражают расходы на продукты и услуги как медицинского, так и немедицинского характера. Косвенные затраты не требуют указания прямых расходов, однако они, безусловно, имеют экономическую составляющую.
Таблица 2Категории затрат при исследовании исходов лечения
Виды затрат | Примеры затрат |
Прямые медицинские затраты (товары и услуги) | · Госпитализация |
Прямые немедицинские затраты (требующиеся в связи с заболеванием) | · Питание |
Косвенные затраты (имеющие экономическую составляющую) | · Потеря трудоспособности |
Экономическая составляющая по отношению к обществу. Учреждениям здравоохранения и другим государственным учреждениям небезразличны затраты, обусловленные тем или иным заболеванием или лечением, равно как и их влияние на качество жизни. При проведении исследований, имеющих подобную социальную составляющую, исследователи должны подсчитывать все прямые и косвенные затраты.
Для достижения большей гибкости в использовании получаемых данных важно отделять затраты немедицинские от медицинских. При этом все они должны отразиться в социальной составляющей, поскольку даже косвенные затраты оказывают влияние на общество через соответствующие налоги и снижение трудоспособности.
Экономическая составляющая со стороны плательщика. Государственные и частные страховые компании — это фактические покупатели оплачиваемых видов лечения. Их основная забота — прямые медицинские затраты. Прямые немедицинские затраты имели бы для них значение только в том случае, если бы страховка покрывала и эти затраты. Организации, оказывающие медицинские услуги, и другие учреждения здравоохранения являются страхователями. Они берут на себя ту долю экономической составляющей со стороны плательщика, которая обусловлена прямыми медицинскими затратами.
Государственные органы медицинского страхования интересуют затраты на лечение на длительную перспективу. Если сегодня стоимость лечения высокая, но в течение жизни она имеет тенденцию к снижению, то органы страхования в будущем получат экономическую выгоду.
Так, в США члены организаций медицинского обслуживания (Heath Maintenance Organizations — НМО) считают необходимым изменять свои планы в среднем один раз в два года, что ограничивает интерес страхователей этих организаций к инвестициям в дорогостоящие виды лечения с целью сэкономить финансовые средства в будущем.Экономическая составляющая со стороны организаций, оказывающих медицинские услуги. Врачи, занимающиеся частной практикой, традиционно не интересуются затратами на лечение, особенно если пациенты застрахованы в частном порядке. С точки зрения экономической составляющей, их больше интересуют факторы, влияющие на качество жизни пациента. Некоторые учреждения здравоохранения, такие, как организации обеспечения медицинской помощью, а также врачи системы государственного здравоохранения одинаково оценивают значение обоих аспектов экономической составляющей — как со стороны учреждений здравоохранения, так и со стороны плательщиков — поскольку они и организуют медицинскую помощь, и оказывают необходимые медицинские услуги. Врачи частной практики в тех странах, где существует государственная система страхования здоровья, должны оказывать медицинские услуги, уделяя основное внимание экономической составляющей. И частным, и государственным медицинским учреждениям далеко небезразлично качество жизни пациентов, но их деятельность в большей степени мотивирована уровнем затрат на медицинское обслуживание.
Экономическая составляющая со стороны пациента. В целом факторы, влияющие на качество жизни, наиболее важны для пациента, особенно при наличии страховки или членства в системе государственного здравоохранения. С точки зрения экономической составляющей, для пациента наибольшее значение имеют не компенсируемые расходы, которые обычно составляют прямые немедицинские затраты, а косвенные личные затраты. В тех пределах, в которых пациент имеет возможность выбирать вид лечения, он, вероятно, предпочтет лечение, которое принесет максимальную пользу с точки зрения качества жизни независимо от затрат. Личные предпочтения пациента имеют решающее значение при принятии решения о лечении как со стороны врачей частной практики, так и со стороны государственных учреждений здравоохранения.
Информация о видах затрат и влиянии лечения, полученная в ходе клинических исследований исходов лечения и имеющая наибольшее значение для каждой из сторон, обобщена в табл. 3. Необходимо иметь в виду, что та или иная сторона принимает во внимание более чем одну экономическую составляющую.
Таблица 3Информация об экономической составляющей лечения
Экономические составляющие исследования | Наиболее существенные затраты |
Общество | · Все прямые кратковременные и косвенные затраты |
Плательщики | · Прямые кратковременные затраты |
Услуги учреждений здравоохранения | · Влияние на качество жизни |
Пациент | · Влияние на качество жизни |
Фармакоэкономические исследования в процессе клинической разработки. Для фармацевтической компании существует два варианта изучения исходов лечения: 1-й — сбор данных об исходах лечения в рамках традиционной системы клинических испытаний, 2-й — сбор данных независимо от этой системы. Использование данных об оценках фармакоэкономического анализа в процессе проведения клинических разработок имеет как положительные, так и отрицательные стороны.
Положительные стороны одновременного проведения фармакоэкономического анализа и клинических разработок:
Представляется более эффективным собирать данные об испытуемых, уже вовлеченных в процесс научного исследования.
Одновременное выполнение двух задач научного исследования дает возможность проводить фармакоэкономическое исследование по плану параллельных групп.
Данные об эффективности и безопасности лекарственных средств можно напрямую сравнивать с данными об оценке как экономических факторов, так и качества жизни, получаемых непосредственно от пациентов.
Показатели качества жизни с большей вероятностью будут надежными и обоснованными, если испытуемые будут отобраны по принципу случайной выборки.
Отрицательные стороны одновременного проведения двух типов исследования:
Трудно оценить эффективность предоставления медицинских услуг вне естественных условий. Визиты, ограниченные требованиями Протокола, искажают общую картину эффективности медицинского обслуживания пациента, а следовательно, и представление о затратах. Например, испытуемый, озабоченный вопросом оплаты, может ждать очередного запланированного визита вместо того, чтобы обратиться к врачу самому либо связаться с ним по телефону и задать интересующие вопросы. Экономическая эффективность, оцениваемая по контрольным клиническим испытаниям препарата, не будет надежно обоснована.
Исследователи отрицательно относятся к сбору дополнительных данных, которые могут расцениваться как не имеющие отношения к делу.
Многие клинические испытания могут оказаться недостаточно продолжительными, чтобы оценить влияние лечения на качество жизни в течение длительного времени. Их продление для получения подобных результатов привело бы к продлению сроков разработки препарата. Этого можно избежать, продолжая сбор данных о результатах экономического характера после того, как сбор данных по клиническим параметрам уже завершен.
Технология моделирования использует положения из области экономики и психологии поведения для прогнозирования последствий, которые могут иметь место в реальной жизни. Вы можете накапливать соответствующую информацию, на основе которой специалист, который проводит фармакоэкономический анализ, может моделировать итоговые оценки, имеющие реальное экономическое содержание. Благодаря построению модели на основе исходных данных эта информация может стать более достоверной. Однако имеются различия в оценке приемлемости технологии моделирования со стороны муниципальных органов и учреждений здравоохранения. Специалист, который проводит фармакоэкономический анализ, знает, в какой степени технология моделирования может помочь вам при проведении клинического исследования в конкретной стране или международного исследования.
Результаты исследования привлекают гораздо больше внимания, нежели исследовательская деятельность как таковая. Частично это происходит в силу низкой осведомленности. В то же время это объясняется наличием таких негативных обстоятельств:
фармакоэкономическое исследование может быть очень дорогостоящим;
фармакоэкономические исследования могут продолжаться в течение нескольких лет, если задача оценить их ставится на долговременную перспективу;
еще никому не удалось точно установить, какую информацию будут использовать плательщики, учреждения здравоохранения и ценообразующие органы в качестве решающей;
до настоящего времени не разработана общепризнанная модель оценки фармакоэкономических исследований;
дорогостоящее и длительное исследование — рискованный шаг, если результаты непредсказуемы. Обнаружение безопасного и эффективного средства, по критерию эффективности затрат имеющего более низкий коэффициент по сравнению с другим средством, могло бы положительно отразиться на потенциале рынка;
фармакоэкономические исследования находятся сейчас в процессе развития, и на этом пути редко можно встретить полное взаимопонимание.
Использование данных о фармакоэкономических исследованиях при разработке проектных планов. Организация, проводящая фармакоэкономические исследования, должна быть хорошо оснащена. Необходимы специализированные группы, оказывающие помощь руководителям проектов в планировании и проведении фармакоэкономических исследований. По мере определения потребностей и возможностей для исследований нового препарата следует подобрать или пригласить соответствующих специалистов и консультантов в вашу организацию. В процессе разработки продукта необходимо рассмотреть экономические аспекты его применения.
Уже на самом раннем этапе планирования клинической разработки и маркетинга необходимо проанализировать экономические аспекты использования нового средства. Если отсутствуют данные о затратах при его использовании по показаниям, следует провести соответствующее клиническое исследование. Если экономические преимущества препарата неизвестны, целесообразно организовать исследования по технологии моделирования и вероятностного прогнозирования до начала полномасштабного исследования. Данные по затратам на лечение (анализ всех издержек) могут помочь в прогнозировании уровня этих затрат, обеспечивающего продвижение лекарственного препарата на рынок.
Использование результатов фармакоэкономического исследования
Продвижение на рынок более перспективного лекарственного препарата по сравнению с используемыми на практике.
Поддержка больниц, государственных медицинских учреждений и организаций медицинского обслуживания в принятии необходимых решений по формированию формуляров лечения.
Обеспечение отдельных лиц и организаций, осуществляющих закупку лекарственных средств, необходимыми данными по вопросам ценообразования.
Установление приемлемых цен на лекарственные средства в странах, имеющих органы ценообразования.
После определения приемлемых способов применения результатов исследования по лекарственному препарату необходимо получить консультацию специалиста, проводившего фармакоэкономическое исследование. Конечные результаты экономического характера могут быть менее объективными по сравнению с конечными результатами исследования эффективности лекарственного средства. Опираясь на обоснованные экономические критерии, опытный эксперт определит разницу между исследованием, имеющим незначительный эффект (или не имеющим такового), и исследованием с обоснованными положительными результатами. Специалисты по фармакоэкономическим исследованиям располагают информацией относительно обоснованных и надежных критериев оценки экономического характера. Они могут разработать метод экономического анализа, способный обеспечить достижение целей соответствующего клинического исследования.
Новые тенденции регулирующих органов различных стран. В настоящее время правительства различных стран в сотрудничестве c представителями местной фармацевтической промышленности разрабатывают Правила экономической оценки лекарственных средств для производителей. Несмотря на различия в порядке ценообразования и компенсации затрат на лекарственные средства в разных странах, эти разработки имеют некоторые общие черты. Наиболее важное свидетельство интереса к таким Правилам — предоставление экономических данных для обоснования заявок на компенсацию затрат на лекарственные средства. Для фармацевтической промышленности стало общим правило предоставления информации не только о безопасности, эффективности и качестве новой продукции, но и о ее стоимости. В результате этого требования экономический анализ лекарственных средств получил более широкое распространение.
Правила экономической оценки лекарственных средств могут служить различным целям. В Австралии от фармацевтических фирм требуется проведение экономической оценки в случае, если они выходят с заявкой о возмещении затрат на свою продукцию. Правила могут быть использованы в целях применения методических и этических стандартов в практике экономической оценки лекарственных средств, что позволяет обойтись без официального давления. Правительство получает выгоду от введения данных Правил, поскольку их можно использовать для контроля расходов на лекарственные средства или для обеспечения рационального распределения фондов с целью получить наибольшую прибыль. Наконец, содействие повышению эффективности системы выдачи льготных рецептов на лекарственные средства подкрепляет целесообразность введения Правил экономической оценки лекарственных средств. Экономическая оценка лекарственных средств необходима и для формирования национального справочника лекарственных средств, субсидируемых правительством.
Правила, согласно которым результаты фармакоэкономического исследования с помощью анализа эффективности и затрат (СЕА) должны предоставляться после того, как установлены безопасность, эффективность и качество лекарственного средства, могут стать барьером, который необходимо будет преодолеть. С одной стороны, производители могут возражать против дополнительных расходов, обусловленных проведением экономического анализа и предоставлением дополнительных сведений к документам, подаваемым вместе с заявкой на регистрацию лекарства, с другой — согласно Правилам устанавливают стандарты на порядок применения экономических критериев и уточняют процедуру принятия решения о предоставлении субсидий. Кроме того, при наличии конкуренции на фармацевтических рынках экономическая оценка лекарственных средств может оказаться важным инструментом маркетинга. Поэтому промышленность может поддержать их разработку, но официальное требование о введении таких Правил в обычную практику не должно быть обязательным.
В.И. Мальцев, д-р мед. наук, профессор, заведующий сектором координации и контроля клинических испытаний лекарственных средств ГП «Государственный фармакологический центр» МЗ Украины
Т.К. Ефимцева, канд. мед. наук, заместитель заведующего отделом координации и контроля клинических испытаний лекарственных средств ГП «Государственный фармакологический центр» МЗ Украины
Д.Ю. Белоусов, Центр фармакоэкономических исследований, г. МоскваЛИТЕРАТУРА
Gold M.R., Siegel J.E., Russel L.B. at al. Cost-effectiveness in health and medicine, 1996, NY, Oxford University Press.
Клинические испытания лекарственных средств / Под ред. В.И. Мальцева, Т.К. Ефимцевой, Ю.Б. Белоусова, В.Н. Коваленко. — К.: Морион, 2002. — 352 с.
Планирование и проведение клинических исследований лекарственных средств / Под ред. Ю.Б. Белоусова. — М., 2000. — С. 223–260.
Чурилин Ю.Ю. Типы и методы проведения научного анализа исходов // Качественная клиническая практика. — 2001. — № 1. — С. 65–75.
Экономическая оценка эффективности лекарственной терапии (фармакоэкономический анализ) / Под ред. П.А. Воробьева. — М., 2000. — С. 28–48.
Источник: apteka.ua
.png)