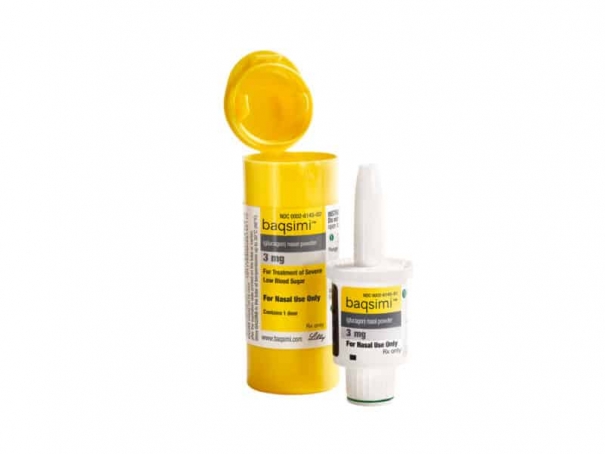
В США зарегистрирован препарат Баксими компании Eli Lilly для купирования тяжелой гипогликемии
- Новости /
-
2939
FDA одобрило препарат Баксими (Baqsimi) компании Eli Lilly and Company в форме порошка для интраназального введения, предназначенный для купирования тяжелой гипогликемии у пациентов с сахарным диабетом в возрасте 4 лет и старше. Это первая терапия глюкагоном, не требующая инъекции.
Тяжелая гипогликемия возникает в случае, когда уровень сахара в крови пациента падает до уровня, когда он теряет сознание или возникают другие симптомы, для купирования которых требуется помощь другого человека. Обычно такое состояние возникает у пациентов с сахарным диабетом, использующих инсулин.
До этого момента на рынке были представлены препараты для купирования тяжелой гипогликемии, которые вводились с помощью инъекции глюкагона, которую сначала нужно было смешать в несколько этапов. Новая форма препарата поможет значительно упростить введение препарата в критических ситуациях.
Препарат Баксими повышает уровень сахара в крови, стимулируя печень выделять накопленную глюкозу в кровь. Он оказывает эффект, противоположный действию инсулина. Эффективность и безопасность лекарственного средства оценивалась в ходе двух клинических исследований с участием 83 и 70 пациентов с сахарным диабетом. Согласно полученным результатам, препарат Баксими смог адекватно повысить уровень сахара в крови. Аналогичные результаты были получены и в ходе исследования с участием 48 детей старше 4 лет с сахарным диабетом. Наиболее распространенными побочными эффектами, связанными с приемом Баксими, были тошнота, рвота, головная боль, раздражение верхних дыхательных путей, слезотечение, покраснение глаз и зуд.
Препарат Баксими не следует принимать пациентам с феохромоцитомой, редкой опухолью надпочечников, или пациентам с инсулиномой, опухолью поджелудочной железы.
Источник: fda.gov
.png)