Минздрав РФ зарегистрировал упадацитиниб для лечения псориатического артрита
- Новости /
-
2991
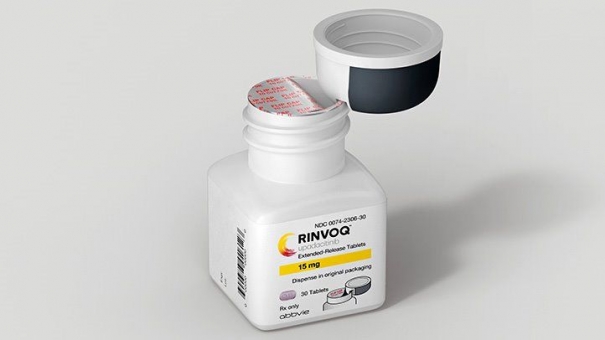
Глобальная научно-исследовательская биофармацевтическая компания AbbVie объявила, что Министерство здравоохранения РФ одобрило препарат Ранвэк (упадацитиниб), пероральный обратимый ингибитор янус киназ в дозе 15 мг один раз в сутки для лечения анкилозирующего спондилита (также называемого Болезнь Бехтерева) и псориатического артрита, тем самым расширяя возможности применения препарата в терапии ревматических заболеваний у взрослых пациентов.
Основанием для одобрения являются результаты трех международных многоцентровых клинических исследований с участием пациентов из РФ, в которых Ранвэк продемонстрировал эффективность по множеству критериев оценки активности этих заболеваний и изученный профиль безопасности упадацитиниба в сравнении с плацебо и адалимумабом.
«Одобрение применения препарата Ранвэк при анкилозирующем спондилите и при псориатическом артрите знаменует важный этап в лечении ревматических заболеваний. — говорит Энтони Вонг, вице президент AbbVie в России и СНГ. — Ранвэк является первым и единственным на данный момент таблетированным таргетным препаратом, одобренным одновременно для терапии ревматоидного артрита, анкилозирующего спондилита и псориатического артрита, что дает пациентам принципиально новый уровень удобства терапии. AbbVie уже более 20 лет разрабатывает программы, направленные на улучшение качества жизни людей, страдающих этими хроническими инвалидизирующими заболеваниями, трудно поддающимися лечению, и мы безгранично рады, что данное одобрение помогает реализовывать нашу главную миссию — оказывать значительное влияние на жизнь пациентов».
В клиническом исследовании SELECT-AXIS 1 2/3-й фазы Ранвэк достиг первичной конечной точки ответа ASAS40 на 14-й неделе по сравнению с плацебо у пациентов с АС, которые имели неадекватный ответ на нестероидные противовоспалительные препараты (НПВП). Кроме того, Ранвэк достиг статистической значимости по таким ключевым вторичным конечным точкам с поправкой на множественные сравнения с плацебо, как частичная ремиссия по ASAS и BASDAI 50 на 14-й неделе.
В клинических исследованиях SELECT-PsA 1 и SELECT-PsA 2 3-й фазы достигнута первичная конечная точка в виде ответа ACR20 на 12-й неделе на фоне терапии Ранвэк в сравнении с плацебо у взрослых пациентов с активным псориатическим артритом, у которых наблюдался неадекватный ответ на базисные противовоспалительные препараты (БПВП) или ГИБП. В исследовании SELECT-PsA 1 была показана не меньшая эффективность по ответу ACR 20 на 12-й неделе для препарата Ранвэк по сравнению с адалимумабом (40 мг, каждые две недели). Также продемонстрировано более выраженное улучшение физической активности (по оценке HAQ-DI на 12-й неделе) и разрешение кожных симптомов (по оценке PASI75 на 16-й неделе), большая часть пациентов достигла минимальной активности заболевания на 24 неделе по сравнению с теми, кто получал плацебо. Профиль безопасности препарата Ранвэк в исследованиях SELECT-AXIS 1, SELECT-PsA 1 и SELECT-PsA 2 полностью соответствовал таковому по уже опубликованным исследованиям программы SELECT. Новых рисков по безопасности не обнаружено.
Источник: https://pharmprom.ru
.png)